除了表观遗传学,新陈代谢也能调节基因表达
基因程序失调会导致癌症和破坏性的炎症反应,揭开基因打开和关闭的调控密码一直是生物医学研究的一个重要目标。
众所周知,细胞代谢能影响基因调控,比如胚胎干细胞的谷氨酰胺代谢会影响细胞分化、DNA表观遗传学以及染色体DNA的解聚或压缩。泛泛的表观遗传学事件是如何精确地转化为具体的基因程序的呢?这是当前知识体系的一大漏洞。
阿拉巴马大学的研究生Danielle Chisolm和微生物学教授Amy Weinmann最近在《Immunity》杂志上报告了谷氨酰胺摄取进入细胞与所选基因程序控制之间联系工作机理。这一发现表明,曾经被认为仅参与产能和细胞基础建设的新陈代谢也可以帮助细胞分化。乳酸可以刺激干细胞,让毛发再生!
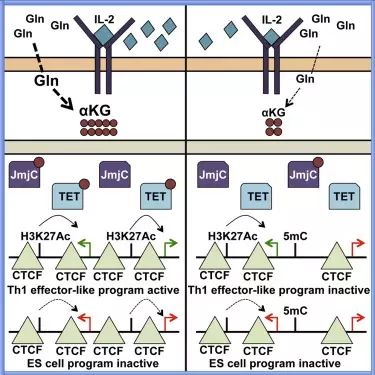
谷氨酰胺的细胞内代谢产物α-酮戊二酸(alpha-ketoglutarate,,αKG)通过转变转录因子CTCF与DNA的结合方式,从而调节细胞分化。作为基因程序控制复杂性的附加级别,研究人员发现,结合位点的基因组上下文(如表观遗传变化或基因组拓扑改变)影响着此次结合的目的——关闭还是开启基因程序。
这篇文章的分子生物学研究策略类似于逆向工程:工程师通过选取机器的一部分,分析其中零件细节,来提取机器的设计方案。研究人员形象地拆解了T细胞(机器),通过调节白细胞介素2改变α-酮戊二酸渗入细胞的水平、添加酶抑制剂、RNAi等手段细致地分析了细胞的工作原理。
“无论正常状态还是疾病状态,我们都想知道DNA是如何表达的?”
Chisolm和Weinmann比较观察了一个T细胞模型系统和胚胎干细胞,发现它们的基因程序控制之间存在一种有趣的联系。
她们注意到,激活辅助性T细胞(T helper 1,Th1)或胚胎干细胞的α-酮戊二酸后,CTCF的一组基因结合位点开始与一些在早期发育时表达的基因关联。
研究人员在胚胎干细胞中发现,三分之一的α-酮戊二酸驱动事件与Th1细胞中经α-酮戊二酸诱导的CTCF结合峰的位置存在关联。因此,科学家们推断胚胎生长期间,其控制位点也可能是控制T细胞遇到免疫挑战后发生改变的调节机制。
不同浓度的白细胞介素2(IL-2)可以驱动细胞打开不同基因程序,这种基因调控过程与效应T细胞或记忆T细胞的基因程序开合十分相似。已知,高水平的白细胞介素2作用于效应T细胞后,同样会驱动新陈代谢变化,包括谷氨酰胺的吸收和代谢降解,让谷氨酰胺在细胞内部富集。
研究人员向低水平表达白细胞介素2的T细胞中加α-酮戊二酸,目的是看有多少基因表达变化是由于α-酮戊二酸诱导的高水平白细胞介素2导致。
他们发现,这种处理方式大概能诱导低水平白细胞介素2T细胞三分之一的基因进程,也会抑制大约10%的基因。α-酮戊二酸似乎参与了一部分,而不是全部的白细胞介素2对T细胞基因编程的影响。
随后研究人员追踪分子线索,采用RNA测序,蛋白质表达测定,染色质免疫共沉淀,Hi-C和生物信息学等技术手段最终发现了差别化的CTCF结合机制。
原文标题
CCCTC-Binding Factor Translates Interleukin 2- and α-Ketoglutarate-Sensitive Metabolic Changes in T Cells into Context-Dependent Gene Programs