BRAFV600突变非黑色素肿瘤的共存基因改变可影响生存?
编译:月下荷花来源:肿瘤资讯
BRAF突变可发生于非黑色素肿瘤中,靶向BRAF的药物却一直未能获批治疗此类肿瘤,这主要源于BRAF抑制剂对BRAF突变非黑色素肿瘤原发或继发耐药,肿瘤中与BRAFV600突变共存的基因改变可能与耐药相关,因此美国Sen教授分析了BRAFV600突变肿瘤的共存基因改变以及改变对BRAFV600抑制剂耐药、肿瘤PFS和OS的影响,研究结果发表在JNCI。
BRAF突变导致MAPK结构性活化,发生于50%皮肤黑色素瘤,10%非黑色素瘤。威罗非尼、考比替尼、达拉非尼和曲美替尼已获FDA批准治疗BRAFV600突变转移性黑色素瘤,治疗反应率超过50%。很多非黑色素肿瘤BRAFV600突变不但与肿瘤侵袭性增强相关,且对靶向BRAFV600的治疗耐药。Sen教授的研究显示PI3K-mTOR途径改变可能在耐药中发挥作用。
2012年~2016年期间,MD Anderson癌症中心共有30例BRAFV600突变非黑色素肿瘤采用BRAF靶向药物治疗且具有NGS数据,对数据采用Kaplan-Meier分析和Cox比例风险回归分析,计算HR,拟明确BRAF抑制剂单药治疗下的生存是否与共存基因改变相关。
30例患者采用BRAFV600抑制剂单药治疗,11例非小细胞肺癌,5例结直肠癌,4例胆管癌,3例甲状腺癌,3例Erdheim Chester病,2例脑胶质瘤,1例涎腺癌和1例来源不明肿瘤。3/5结直肠癌为BRAF抑制剂联合西妥昔单抗,其中2例伴有PI3K-mTOR途径改变。共存基因改变分三种亚型:14例无共存基因改变,5例PI3K-mTOR途径改变,11例伴其它突变,包括TP53(11例)、SMAD4(4例)、LKB1(2例)和IDH1突变(2例)。
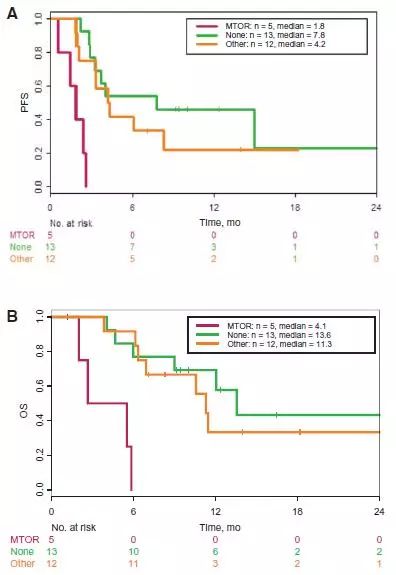
8例有治疗反应且无疾病进展的患者中6例无共存基因改变(PFS 222–805天),所有伴PI3K-mTOR途径改变者都在77天内疾病进展。Kaplan-Meier分析证实伴PI3K-mTOR 途径突变患者的PFS和OS明显低于无共存基因改变或其它突变者(图1),PFS和OS只有1.8个和4.1个月,而伴其它突变者为4.2和11.3个月,无突变者7.8和13.6个月。
图1 BRAF突变非黑色素肿瘤采用BRAF抑制剂单药治疗时的PFS(A)和OS(B),患者分层绿色为不伴改变者,紫色为伴mTOR途径改变者,桔色为伴其它突变者。
BRAF突变、扩增和融合发生在许多非黑色素肿瘤中,通过这项研究发现,这些肿瘤中的共存基因改变至少存在三种亚型,并与肿瘤的PFS和OS相关。大约20%肿瘤具有PI3K-mTOR途径改变,与BRAF抑制剂耐药相关,明显缩短PFS和OS。
黑色素瘤中BRAF靶向治疗耐药与MAPK和PI3K-mTOR途径活化或与免疫系统无效调节相关,这项研究显示,mTOR途径活化或也是非黑色素肿瘤的耐药机制。结直肠癌模型研究也显示,PI3K-mTOR途径活化是结直肠癌BRAF抑制耐药的机制,临床上还显示,BRAF抑制耐药有可能通过EGFR途径介导,在这项研究中尽管加入西妥昔单抗,伴PI3KmTOR途径改变的结直肠肿瘤生存仍很差。
研究不足:
MAPK和mTOR途径存在交叉,因此mTOR活化可能与BRAF靶向治疗获得性耐药相关,这一点需进一步研究,尤其需在疾病进展时再次活检,缺少连续活检结果是这项研究的不足,同时样本量小也会影响结果,BRAF突变非黑色素肿瘤共存基因改变可能有助于预测治疗反应需要更多研究证实,目前一项威罗非尼联合mTOR抑制剂依维莫司的I期研究正在进行中。
评论:
尽管BRAF抑制治疗在黑色素瘤中取得了良好疗效,但在其它非黑色素肿瘤中却没有获得相应治疗效果,明确其发生机制对指导更有针对性的治疗具有重要意义,本文发现mTOR途径改变与BRAF突变共存时可能是耐药的机制,为BRAF抑制与mTOR抑制联合治疗提供了理论基础。
参考文献
https://academic.oup.com/jnci/article-abstract/109/10/djx094/4086475/Co-occurring-Genomic-Alterations-and-Association?redirectedFrom=fulltext
责任编辑:肿瘤资讯-熊熊兔