基因编辑:CRISPR 的竞争者太多,不止有 NgAgo!
CRISPR 系统并不完美,科学家从未停止寻找其他基因编辑工具的脚步。
撰文 Heidi Ledford
翻译 赵琳
审校 赵维杰
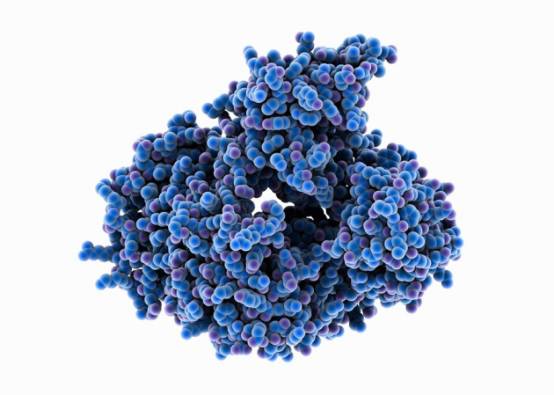
CRISPR-Cas9的潜在竞争者之一:Argonaute。图片来源:SPL
利用 CRISPR-Cas9 技术,科学家们已经可以随心所欲地对基因组进行编辑。和之前的技术相比,它简单、廉价、用途广泛。全世界从事医学与基础科学研究的实验室都对它充满兴趣,不断拓展它的应用。
然而,尽管如此,CRISPR-Cas9 并不完美。加利福尼亚大学圣迭戈分校的生物工程学家 Prashant Mali 认为,“这个系统寻找基因组中指定位置并对其进行精确切割的能力十分出色,“但有时,我们需要的不止这些。”
CRISPR-Cas9 系统的局限性推动着寻找其替代者的工作。今年年初,研究者将目光投向了另一个可能也可以执行基因编辑的系统,NgAgo。哈佛医学院的遗传学家 George Church 表示:新技术都是脆弱的,随时可能被取代。
然而,NgAgo 并不是唯一一种新型的基因编辑工具。这些新工具中,有些改良自 CRISPR 系统;另一些则提供了全新的模式。
1迷你版 Cas9
在将来,CRISPR-Cas9 系统可能会用于基因疗法,改写遗传疾病的相关基因。基因疗法通常使用病毒作为载体,将外源遗传物质运载进入人体细胞。而病毒基因组容量有限,很难容纳 CRISPR-Cas9 系统的全部组分——Cas9 酶,以及引导用的单链 RNA。
一种迷你型 Cas9 酶的发现有可能解决这一问题【1】。这个迷你版来自金黄色葡萄球菌(Staphylococcus aureus),它的序列足够短,可以压缩进当前用于基因疗法的病毒中。去年12月,两个研究组利用迷你版 Cas9 修正了小鼠体内的杜兴氏肌营养不良症(Duchenne muscular dystrophy)的相关基因【2,3】。
2Cas9 的姐妹们
合成生物学家张锋,他的团队不仅在 CRISPR-Cas9 系统的应用领域做出了杰出贡献,也发现了 Cas9 的姐妹:Cpf1。图片来源:Justin Knight Photography
Cas9 并不能切割所有的序列,只有当靶向序列附近存在一段特定的 DNA 序列时,这段序列才能被特异性地切割。这个要求在大部分基因组中都能满足,但对某些实验来说却构成阻碍。研究者们希望能够在微生物中找到 Cas9 的姐妹,在切割过程中它们所需的附近序列与 Cas9 不同,这将可以拓展 CRISPR 系统的应用范围。
Cpf1 就是这样一种酶。它比 Cas9 小,所需要的靶向序列附近的特定 DNA 序列与 Cas9 不同并且高度特异【4,5】。
Cas9 的另一个姐妹 C2c2 则可以切割 RNA 而非 DNA ,这一特性可以用于 RNA 相关领域的研究,或者用来抵御 RNA 病毒【6】。
3真正的基因编辑,不只是敲除
在Cas9基础上改造得到的蛋白具有定点突变功能。图片来源:David R. Liu 实验室网站
在许多实验室里,CRISPR-Cas9 只用来做基因敲除。Church 说:“人们想宣告说这就是基因编辑,然而烧掉书中的某一页并不等于是在编辑这本书。”
比基因敲除更难的,是将一段序列替换为另一段序列。Cas9 切割 DNA 后,细胞中的修复机制常常会错误地将打断的末端连在一起,从而实现基因敲除。
想要改写 DNA 序列的研究者,则希望另外一种修复机制发生,将一段新的 DNA 序列插入到基因组中,然而这种机制发挥作用的几率远小于直接连接。明尼苏达大学的植物科学家 Daniel Voytas 说:“所有人都说,在未来我们将可以一次性编辑多个基因。但我认为,我们现在甚至还不能高效地完成‘一次真正的基因编辑’。”
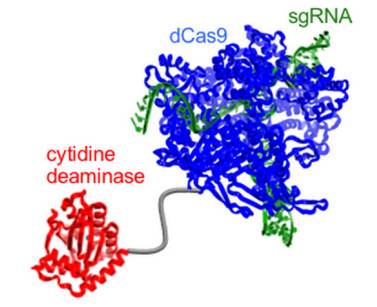
然而,过去几个月中的进展为 Voytas 带来了希望。今年4月有研究者宣布,他们将失活的 Cas9 与一个可以制造 DNA 点突变的酶连接在了一起。失活的 Cas9 仍然可以定位于引导RNA 所指定的序列,但无法完成切割。而此时,与之相连的酶可以制造点突变,将 C 突变为 T 【7】今年8月发表于 Science 杂志的另一篇论文也报道了类似的结果【8】。
Voytas 等人对类似的尝试表示了期待,将失活 Cas9 与不同的酶相连接,可能会完成更丰富多变的序列改变。
4进击的 Argonautes
NgAgo 系统的发明者韩春雨。图片来源:河北科技大学官网
今年五月,发表在 Nature Biotechnology 上的一篇论文【9】报道了一个全新的基因编辑系统。研究者声称能够使用 NgAgo 蛋白在指定位点上切割 DNA ,这个过程使用与目标序列互补的短链 DNA,而非 RNA 作为引导,并且不要求切割位点附近存在某种特异性的序列。
这个发现掀起了一股热潮,不少人认为 CRISPR-Cas9 将会被取代。但目前为止,其他实验室都未能重现该结果。首尔基础科学研究所的基因工程学家 Jin-Soo Kim 认为,即便如此,人们还没有放弃希望,来源于其他细菌的 Argonautes 家族蛋白(NgAgo 是 Argonautes 蛋白家族的成员)有可能会提供新的思路。
5更多可能
其他的基因编辑系统也正在建设中,然而它们中的一部分在过去多年中都进展缓慢。在一个致力于在细菌中进行基因编辑的大规模项目中,Church 的研究组并没有选择 CRISPR 系统。他们主要使用的是一个名为“lambda Red”的系统,经过编码,它可以用来编辑特定的 DNA 序列,而这个过程不需要引导 RNA 的存在。Church 的研究组已经在 lambda Red 系统的研究上花费了13年的时间,但是这个系统依旧只能在细菌中发挥作用。
Church 与博德研究所的生物工程学家张锋都提到,他们的实验室正在研究可以用于基因编辑的整合酶(integrases)与重组酶(recombinases)。张锋说:“通过对多种酶进行探索,我们可以得到一个更强的基因组编辑工具箱。我们必须继续探索未知。”
参考文献:
1. In vivo genome editing using Staphylococcus aureus Cas9. F. A. Ran et al. Nature 520, 186-191 (2015).
2. In vivo genome editing improves muscle function in a mouse model of Duchenne muscular dystrophy. Nelson, C. E. et al. Science 351, 403–407 (2016).
3. In vivo gene editing in dystrophic mouse muscle and muscle stem cells. Tabebordbar, M. et al. Science 351, 407–411 (2016).
4. Genome-wide analysis reveals specificities of Cpf1 endonucleases in human cells. Kim, D. et al. Nature Biotechnol. (2016).
5. Genome-wide specificities of CRISPR-Cas Cpf1 nucleases in human cells. Kleinstiver, B. P. et al. Nature Biotechnol. (2016).
6. C2c2 is a single-component programmable RNA-guided RNA-targeting CRISPR effector. Abudayyeh, O. O. et al. Science 353, aaf5573 (2016).
7. Programmable editing of a target base in genomic DNA without double-stranded DNA cleavage. Komor, A. C., Kim, Y. B., Packer, M. S., Zuris, J. A. & Liu, D. R. Nature 533, 420–424 (2016).
8. Targeted nucleotide editing using hybrid prokaryotic and vertebrate adaptive immune systems . Nishida, K. et al. Science (2016).
9. DNA-guided genome editing using the Natronobacterium gregoryi Argonaute. Gao, F. et al. Nature Biotechnol. 34, 768–773 (2016).
文章来源: Nature 536, 136–137 (11 August 2016) doi:10.1038/536136b
原文链接:
http://www.nature.com/news/beyond-crispr-a-guide-to-the-many-other-ways-to-edit-a-genome-1.20388#/references