中国专家共识:乳腺癌易感基因数据解读
编写组成员
(按单位名称汉语拼音字母顺序排列)
-
北京大学医学部(张波)
-
北京医院(王征)
-
成都军区昆明总医院(杨举伦)
-
第三军医大学大坪医院(肖华亮)
-
第三军医大学西南医院(阎晓初)
-
第四军医大学西京医院(王哲、叶菁)
-
福建省肿瘤医院(陈刚)
-
复旦大学附属妇产科医院(赵晨燕)
-
复旦大学附属中山医院(侯英勇)
-
复旦大学附属肿瘤医院(周晓燕)
-
复旦大学医学院(朱虹光)
-
广东省人民医院(刘艳辉)
-
哈尔滨医科大学附属第一医院(吴鹤)
-
河北医科大学第四医院(刘月平)
-
河南省肿瘤医院(马杰)
-
华中科技大学同济医学院(段亚琦)
-
吉林大学第二医院(孙平丽)
-
江苏省人民医院(张智弘)
-
解放军总医院(石怀银)
-
南方医科大学南方医院(梁莉)
-
南京军区南京总医院(饶秋、周晓军)
-
山东省肿瘤医院(穆殿斌)
-
山西省肿瘤医院(郗彦凤)
-
上海交通大学附属胸科医院(张杰)
-
上海交通大学附属新华医院(王立峰)
-
同济大学附属上海肺科医院(武春燕)
-
首都医科大学宣武医院(滕梁红)
-
四川大学华西医院(步宏、刘卫平、叶丰)
-
天津医科大学肿瘤医院(付丽、李帅)
-
天津医科大学(张丹芳)
-
西安交通大学附属第一医院(张冠军)
-
浙江大学医学院(毛峥嵘)
-
浙江大学附属第一医院(丁伟)
-
浙江大学附属邵逸夫医院(许颂霄)
-
浙江省肿瘤医院(孙文勇)
-
郑州大学第一附属医院(姜国忠)
-
中国科学院计算技术研究所(赵屹)
-
中国医科大学附属第一医院(邱雪杉)
-
中国医学科学院协和医院(梁智勇、吴焕文)
-
中国医学科学院肿瘤医院(应建明)
-
中南大学湘雅医院(周建华)
-
中山大学附属第一医院(王连唐)
-
中山大学附属肿瘤医院(邵建永)
-
中山大学肿瘤防治中心(左志向)
执笔作者:吴焕文,叶丰
基金项目:科技部卫生行业科研专项基金(201402001)
原文参见:中华病理学杂志. 2017;46(5):293-297.
乳腺癌易感基因(BRCA)是重要的抑癌基因与肿瘤易感基因,包括BRCA1及BRCA2。BRCA在DNA修复的同源性重组机制中扮演重要角色,BRCA基因突变会导致基因组不稳定性显著增加。胚系BRCA1/2突变(gBRCAm)将显著提高女性乳腺癌、卵巢癌以及其他癌症的发病风险。近年来的研究发现,在一小部分无胚系BRCA基因突变患者的乳腺癌或卵巢癌肿瘤组织中也可以检测到BRCA基因体细胞突变(sBRCAm)。BRCA基因也是与精准治疗密切相关的生物标志物,具有BRCA1/2突变的卵巢癌患者对铂类化疗非常敏感,预后良好,并可获益于聚二磷酸腺苷核糖聚合酶(PARP)抑制剂的治疗【1】。随着精准医学和靶向治疗的进展,对相关肿瘤患者血液和/或肿瘤组织进行BRCA突变检测将有助于更好地判断预后、选择靶向药物、选择化疗方案、在适当的条件下对家族遗传史患者亲属的患病风险进行评估,帮助医师根据患者的基因状态来选取更精准的治疗方案。
BRCA1/2基因序列较长,变异形式多样,变异位点分散遍布于2个基因的全长【2】,并且不是所有的BRCA变异都会损伤蛋白质功能,因而,变异的解读是BRCA检测中一个关键的环节。BRCA基因变异解读需要依据各类信息(包括来自群体数据库、疾病数据库、文献和患者病史的信息)进行综合评判。近年来国外多个权威机构先后发布了BRCA基因变异数据解读的标准或指南。目前,我国在BRCA基因变异数据解读领域尚缺乏规范性指导。因此,中华医学会病理学分会特组织分子病理学领域的相关专家进行了充分讨论,并形成共识发布,以指导与规范我国BRCA基因检测数据的解读,推动BRCA检测在我国的临床应用。
1 BRCA变异类型、检测区域及检测方法
BRCA变异类型主要包括点突变、小片段插入/缺失和大片段重排等。除BRCA基因编码区的变异外,内含子发生的一些变异亦可能会通过干扰RNA剪切等方式影响蛋白质功能,因此BRCA检测必须同时覆盖编码区和相邻边界区(以±20bp为佳)。
Sanger测序是检测BRCA基因点突变和小片段插入缺失的传统技术,也可以作为其他检测方法的补充或结果验证手段。多重连接依赖性探针扩增(MLPA)、定量聚合酶链反应(qPCR)和长片段聚合酶链反应(L-PCR)是目前用于检测BRCA基因大片段重排的三个主要技术平台。
近年来,随着二代测序(NGS)技术的飞速发展,国内外越来越多的实验室已将NGS技术应用于BRCA基因变异的临床检测。除应用于点突变和小片段插入缺失的检测外,在测序策略和生物信息学工具方面有着特殊设计的NGS也可用于大片段重排的检测。
2 BRCA基因变异命名规则
推荐使用人类基因组变异学会(HGVS)命名法作为基因变异命名的主要指导原则以规范基因序列变异的命名。同时参考序列必须包含在内以确保基因变异命名的准确无误。HGVS命名法的首选DNA编码参考序列是基因座参考基因组序列(LRG,www.lrg-sequence.org),但LRG尚未被广泛应用在解读的数据库和文献里。因此根据目前的情况,推荐使用最常用的2个转录本序列,分别为NM_007294.3(BRCA1)和@@NM_000059.3(BRCA2),相应的蛋白质参考序列为NP_009225.1(BRCA1)和@@NP_000050.2(BRCA2)。同时推荐使用命名工具(www.mutalyzer.nl)对基因变异的HGVS命名进行校验。
3 BRCA变异分类
根据国际癌症研究机构(IARC)【3】、美国医学遗传学与基因组学学会(ACMG)【4,5】和胚系突变等位基因解读实证联盟(ENIGMA,www.enigmaconsortium.org)【6】的分类系统,将BRCA基因变异按照风险程度由高至低分为以下5类:致病性(5类,致病可能性>0.99)、可能致病性(4类,致病可能性在0.95~0.99之间)、意义未明(3类,致病可能性在0.05~0.949之间)、可能良性(2类,致病可能性在0.001~0.049之间)和良性(1类,致病可能性<0.001)。受试者的总体BRCA状况应为其所有BRCA1/2基因变异中风险程度最高的类别。
4 BRCA变异解读
目前,BRCA变异解读最权威的指南或标准包括:ACMG和美国分子病理学会(AMP)序列变异解读标准和指南(2015版)【4】,欧洲分子基因诊断质量联盟(EMQN)遗传性乳腺癌/卵巢癌分子遗传分析最佳实践指南(2008版)【7】和ENIGMABRCA1/2基因变异分类标准(1.1版)【6】。
ACMG于2000年发布了第1版变异解读总体指南,并于2007年进行了修订,2015年ACMG和AMP联合发布了该变异解读指南的最新版本。EMQN是一家为全球实验室提供室间质量评定服务的非营利性机构,致力于提高临床分子遗传学检测质量。1999年EMQN起草了第1版遗传性乳腺癌/卵巢癌分子遗传分析最佳实践指南,并于2007年EMQN研讨会讨论,后在2008年更新了该指南。ENIGMA是一个国际研究者联盟,致力于确定BRCA1、BRCA2和其他已知或可疑乳腺癌基因序列变异的临床意义。基于已发表的指南(包括ACMG2007版)和各成员制定的分类标准,ENIGMA于2015年发布了专门针对BRCA1/2的变异分类标准。在其标准里,ENIGMA根据已知的对功能域的认知,总结了BRCA1/2的功能域以及可能恢复BRCA1/2基因功能的自然存在的框内RNA异构体(表1)。除此之外,ENIGMA还发表了一些针对临床意义未明变异的研究。这些都是变异解读非常有用的资源。同一变异依据不同的解读指南或标准所得到的解读结果可能会略有差异,因而我们建议在变异解读时具体指明所依据的指南或标准名称。
综合以上指南解读规则以及BRCA基因的特征,我们总结出以下解读规则:
4.1 致病性5类。包括以下几种情况:
-
编码提前终止密码子的序列变异,即BRCA1第1855位氨基酸和BRCA2第3309位氨基酸前发生的无义突变或移码突变。
-
发生在剪切位点即外显子上下游第一或第二个碱基的变异,但是,需除外经预测或已明确的可产生可能恢复BRCA1/2基因功能的自然存在的框内RNA异构体的变异(表1)。
-
拷贝数缺失变异,该变异导致BRCA1第1855位氨基酸和BRCA2第3309位氨基酸前发生移码突变,或者该变异移除1个或多个外显子且不是经预测或已明确的可产生可能恢复BRCA1/2基因功能的自发框内RNA异构体的变异。
-
任意大小的拷贝数重复变异,该变异导致1个或多个外显子重复并已被证实会导致BRCA1第1855位氨基酸和BRCA2第3309位氨基酸前发生移码突变。
-
体外或体内功能研究显示对基因或基因产物有破坏作用且与肿瘤高危相关的其他类型变异。
4.2 可能致病性4类。包括以下几种情况:
-
该变异经mRNA水平的实验证实能够改变剪接,但是不会产生可能恢复基因功能的自然存在的框内RNA异构体。
-
该变异编码的氨基酸改变与之前定义的5类致病性错义突变相同,但发生改变的基础核苷酸不同,而且既往疾病关联并非由剪接事件所致,并且变异未见于作为对照的外显子组测序项目、千人基因组计划或外显子组整合数据库,或变异位于已确认的功能区。
-
移除密码子的小片段框内缺失变异,该变异涉及的氨基酸位点已被证实可发生错义替换5类变异,且既往疾病关联并非由于剪接事件所致,并且变异未见于作为对照的外显子组测序项目、千人基因组计划或外显子组整合数据库,或变异位于已确认的功能区。
-
体外或体内功能性研究显示对基因或基因产物有破坏作用的其他类型变异,并且变异未见于作为对照的外显子组测序项目、千人基因组计划或外显子组整合数据库,或者变异位于已确认的功能区。
4.3 意义未明3类:证据不足以将其归类为1、2、4或5类的变异,或证据与良性和致病性分类相矛盾的变异。
4.4 可能良性2类。包括以下几种情况:
-
该变异编码的氨基酸改变与已确认的1类良性变异相同,但发生改变的基础核苷酸不同,且无证据表明该变异会导致剪接事件。
-
个体发生的胚系变异与已知致病变异在同一基因上呈反式排列,且该个体除了BRCA相关肿瘤外无明显其他临床表征。
4.5 良性1类:
-
外显子组测序项目、千人基因组计划或外显子组整合数据库中等位基因频率>5%的变异。
-
体外或体内功能研究显示对蛋白质功能或剪接无破坏作用的变异。
5 BRCA变异解读数据库
变异解读的关键步骤之一是收集证据,并基于这些证据对变异进行分类。数据库是挖掘这些证据的重要资源。表2列出了一些常用的数据库,依使用情况分为2类:群体数据库和BRCA相关数据库。群体数据库记录的是以种群为基础的研究中发现的变异。大群体中的变异频率可从此类数据库中获取。BRCA1/2变异相关研究已开展多年,有一些专门收集BRCA变异的数据库和积累大量BRCA变异的疾病数据库,可从中找到变异解读和相应的支持证据。
6 BRCA检测报告
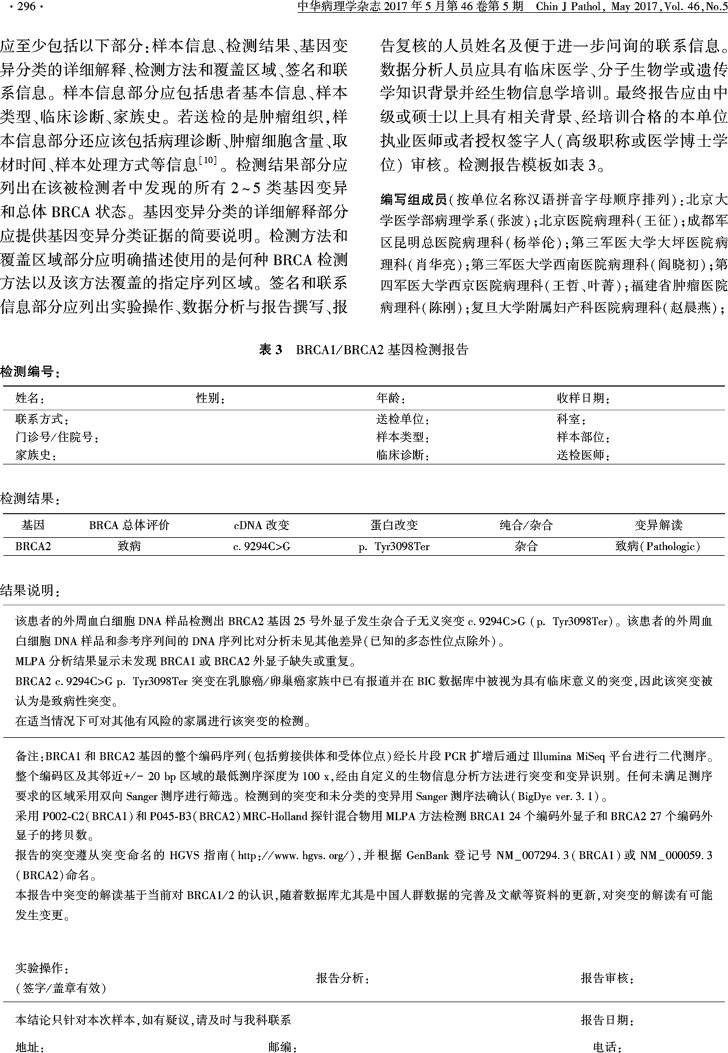
一份完整的BRCA检测报告要能够被肿瘤科医师或其他非分子病理学专业的医师理解,报告内容应至少包括以下部分:样本信息、检测结果、基因变异分类的详细解释、检测方法和覆盖区域、签名和联系信息。样本信息部分应包括患者基本信息、样本类型、临床诊断、家族史。若送检的是肿瘤组织,样本信息部分还应该包括病理诊断、肿瘤细胞含量、取材时间、样本处理方式等信息【10】。检测结果部分应列出在该被检测者中发现的所有2~5类基因变异和总体BRCA状态。基因变异分类的详细解释部分应提供基因变异分类证据的简要说明。检测方法和覆盖区域部分应明确描述使用的是何种BRCA检测方法以及该方法覆盖的指定序列区域。签名和联系信息部分应列出实验操作、数据分析与报告撰写、报告复核的人员姓名及便于进一步问询的联系信息。数据分析人员应具有临床医学、分子生物学或遗传学知识背景并经生物信息学培训。最终报告应由中级或硕士以上具有相关背景、经培训合格的本单位执业医师或者授权签字人(高级职称或医学博士学位)审核。检测报告模板如表3。