癌症治疗的新曙光:基因治疗深度科普
尚方慧诊 国内外肿瘤就医智慧之选
北京上海就医:国内排名前十综合医院和排名前三肿瘤专科医院一站式就医服务(专家门诊挂号预约到治疗陪护等),基因检测及解读等。日本美国就医:日本美国专家会诊/日本美国质子重离子治疗,抗PD1、TAS102等药物治疗。专家远程会诊:北京上海、日本美国资深肿瘤专家远程咨询会诊,以及专家第二意见咨询。
前 言
我们一直说癌症是由于基因异常引起的疾病,近期很多人的微信朋友圈估计都被视网膜疾病的基因疗法刷屏了。基因疗法的受益者之一就是图片的这位25岁的美国姑娘Allison Corona。
因为遗传性眼部疾病莱伯先天性黑朦,Allison Corona的生活一直被笼罩在黑暗中。她几乎认不出颜色,只能看到人的轮廓,但看不到人们的面部特征和表情。直到2012,她参加了一项临床试验,接受了一种叫做基因疗法。现在她25岁了,她说视力有了很大的提高,能看到纹理。只要看到母亲的脸,她就能知道母亲是高兴还是伤心,这在以前是绝不可能的。
Corona接受的基因疗法,有可能从临床试验走向临床使用。近期一个独立的专家委员会以16:0投票一致通过,推荐FDA批准的SparkTherapeutics 公司的luxturna基因疗法。FDA最晚将在2018年1月12日之前决定是否审批。
8月份当诺华的CAR-T获得FDA审批治疗血液癌症的时候,宣传稿中铺天盖地的都是“首个基因疗法”。但是实际上CAR-T是通过对病人自身免疫细胞进行基因改造来治疗癌症,和Corona接受的基因治疗是完全不同的。
可能大家的疑惑就来了:基因治疗到底是怎么一回事呢?是最近才出现的黑科技吗(并不是)?和目前大热的CAR-T等细胞免疫治疗有什么区别吗?基因治疗会造福癌症患者吗?
什么是基因及基因突变?
人体由数万亿个细胞组成。细胞是所有生物的基本组成部分。每个细胞的指挥中心叫做细胞核,它包含染色体。染色体是由身体的遗传物质DNA构成的。
基因是DNA的片段。
通常,每个人的每个基因都有2个拷贝,各自来自父亲和母亲。
得益于人类基因组计划(Human Genome Project),研究人员现在已经找出了人体内的20000多个基因。大多数人的基因都是一样的。然而,每个人都有一小部分基因略有不同。这些基因上的细微差别就是为什么人们有不同的特征(例如身高、皮肤颜色等)的原因。
要了解基因治疗学的复杂性,你首先需要知道我们身体的遗传异常是如何产生的。
基因突变
我们的基因,从父母传给孩子,基因由核糖核酸分子组成的大分子物质,基因编码指导生蛋白质的生成,在细胞中实现绝大部分功能。例如,蛋白质可以制造骨骼,让肌肉运动,控制消化,使心脏跳动。
如果一个基因的DNA序列发生变化,称为突变,例如替换、缺失或复制等。这可能导致一种必需的蛋白质不能正常工作或不能产生一些蛋白质。突变可以从父传给子代,也可以在人的一生中后天获得。而遗传性疾病是一种可以通过基因全部或部分的改变或突变而引起的疾病,这种基因异常会影响产生蛋白的能力,从而造成机体的功能异常。
癌症这一大类疾病,根本患病原因也是基因异常导致的,按照目前科学家的理解,少部分原因是因为遗传基因的异常引起的,绝大部分主要是后天获得的基因异常引起的。了解癌症和基因的关系可以阅读文章读懂基因,更好的了解癌症,癌症和遗传的关系可以阅读文章癌症会遗传吗?
基因的一些变化是无害的,但其他的变化会影响我们的健康。基因突变可能导致遗传疾病。
什么是基因治疗?和CAR-T细胞治疗有什么区别?
简单地说,基因疗法是治疗或预防遗传疾病的医学方法。基因治疗研究的目标是确定一个新的基因是否可以用来替代或失活一个突变的基因来治疗疾病或帮助身体抵抗疾病。
基因治疗研究不是最近才出现的新领域。事实上,科学家们已经研究并发展基因治疗50多年了。
基因治疗研究有可能找到治疗许多疾病的方法,其中一些疾病部分或完全由基因突变引起,例如:
人们可能会混淆基因疗法和细胞疗法。两者都是用来治疗疾病的,但它们是不非常不一样的。
-
细胞疗法是将整个细胞移植到一个人身上,例如CAR-T。了解细胞治疗的更多信息可阅读天价的诺华CAR-T疗法。
-
基因治疗通过将遗传物质引入不能正常工作的细胞或使得细胞更好地工作的方式来操纵细胞。
这意味这什么呢?基因治疗研究的目标是确定一个新基因是否可以用来替换或灭活一个突变基因,以治疗或预防基因疾病。下面的图表代表一个基因的DNA序列的一部分。研究人员正在测试基因疗法的几种潜在方法,包括:
-
提供一个导致疾病的变异基因的健康拷贝
-
向人体引入新的基因
-
抑制或“剔除”一种功能不正常的编译基因
为了将基因传递到细胞中,通常使用一种叫做“载体”的工具来进行转运。
载体的作用:
-
常用的载体可由一种变异病毒制成。
-
在病毒被用作载体之前,它的病毒基因会被移除。
-
一旦病毒被修饰,其目的是将所需的基因运送到细胞而不至于引起疾病。
-
一旦进入体内,所需的基因就应该恢复蛋白质的功能。
载体可以通过静脉注射,或者注入体内的特定组织。其他手段如外科手术,也可用于将载体输送到身体的特定区域。
基因治疗是发生在基因层面上:整体上来讲,细胞是比基因大得多的单位。
而CAR-T治疗是发生在细胞层面上:将整个T细胞提取出来,在体外重新编程,以识别和对抗癌细胞和表达特定抗原的其他细胞。
相同的是基因治疗和CAR-T细胞治疗都是使用病毒作为载体的。
聚焦于眼部遗传性疾病(IRDs)的基因治疗
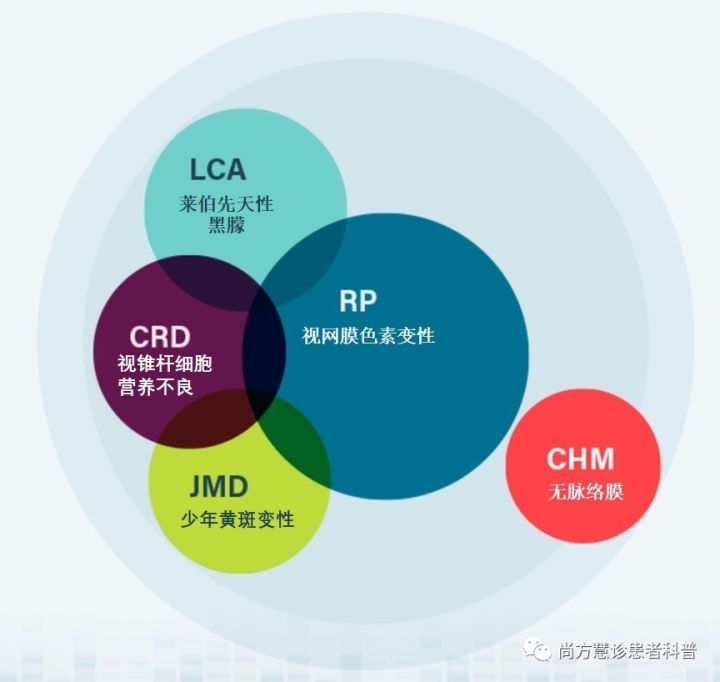
遗传性视网膜疾病(IRDS)是一组疾病:
遗传性视网膜疾病(也被称为遗传性视网膜营养不良,或IRDS)是一组罕见的、由遗传性基因突变引起的眼部疾病,可导致视力下降或失明。
遗传性视网膜疾病的一些人,比如那些有视网膜色素变性(RP)或无脉络膜(CHM)的人,会经历视力的逐渐丧失,最终导致完全失明。其他人,例如莱伯先天性黑朦(LCA),可能是先天的或在婴儿期或儿童早期就会经历视力的丧失。
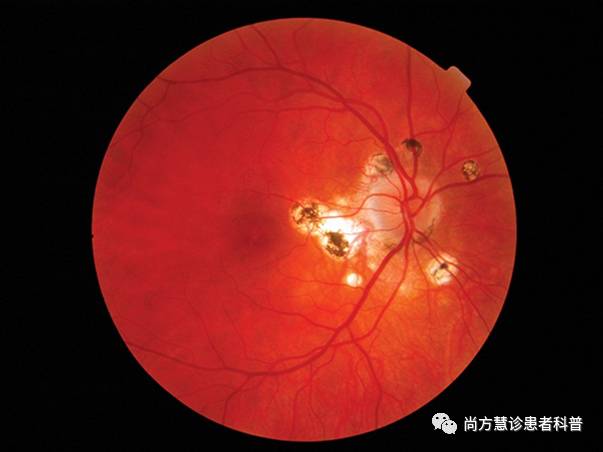
文章一开始提及的被基因治疗改善了视力的姑娘Allison Corona患的就是莱伯先天性黑朦(LCA)。LCA在婴儿期或幼儿期出现,多于19个基因突变会导致这种疾病,LCA会导致婴儿严重视力受损,最终导致儿童失明。婴儿经常有“眼睛蠕动”(眼球震颤,或非自主的眼球来回转动),夜盲症症状,光敏感度降低,并总是用他们的手指揉或按眼睛。
利用病毒载体传递健康基因的拷贝。
研究人员将一个健康的基因复制到病人视网膜细胞的一种方法是使用载体。一些最常见的载体是由变异的病毒制成的。病毒通常被用作载体,因为它们具有进入特定细胞的自然能力。
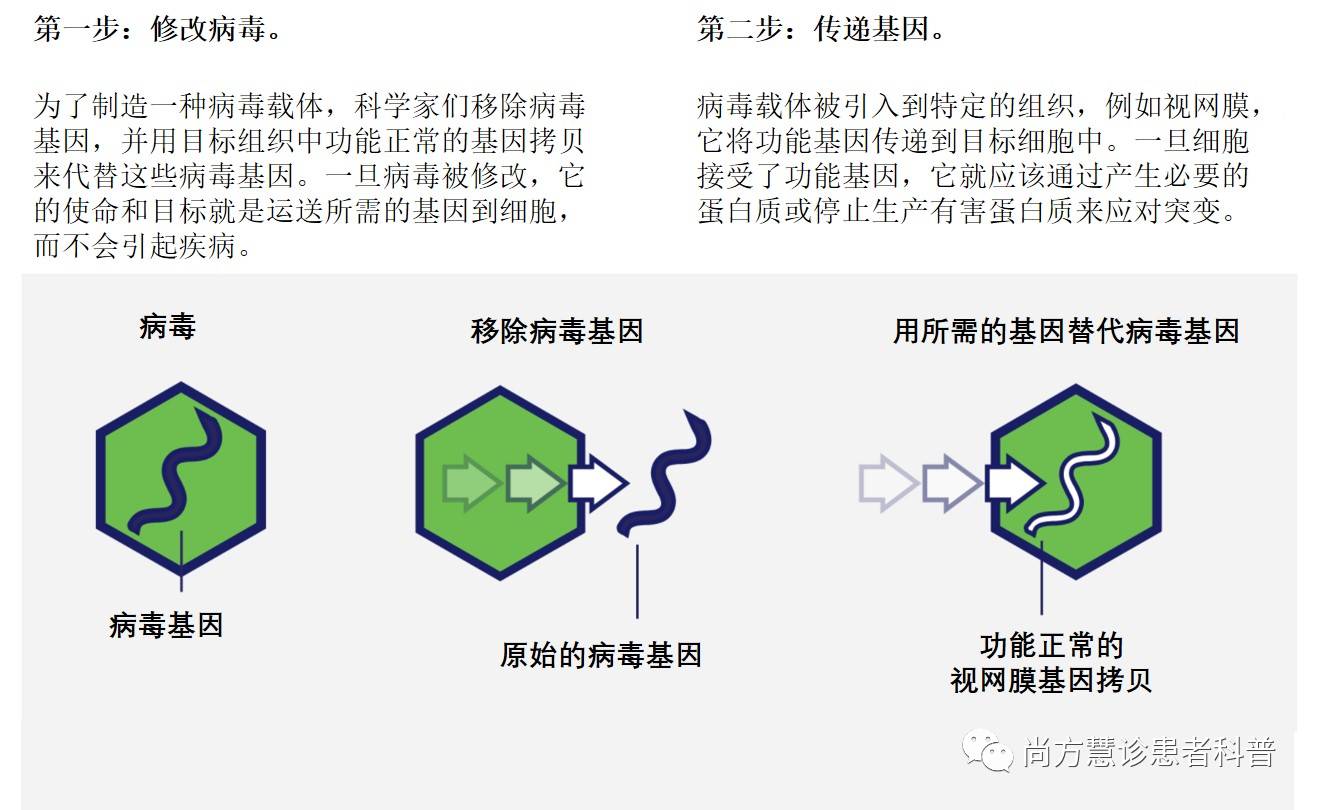
第一步:修改病毒。
为了制造一种病毒载体,科学家们移除病毒内的致病基因,并用目标组织中功能正常的基因拷贝来代替这些病毒基因。一旦病毒被修改,它的使命和目标就是运送所需的基因到细胞,而不会引起疾病。
第二步:传递基因。
病毒载体被引入到特定的组织,例如视网膜,它将功能基因传递到目标细胞中。一旦细胞接受了功能基因,它就应该通过产生必要的蛋白质或停止生产有害蛋白质来应对突变,从而对疾病起到根本的治疗作用。
Spark Therapeutics公司的luxturna基因疗法,能将健康的RPE65基因引入患者体内,让患者能生成具有正常功能的蛋白,从而改善视力。它不但有望治疗艾莉森的莱伯先天性黑蒙症,还能够治疗由RPE65基因突变引起的其他眼疾。
视网膜基因疗法的进展及价格如何?
Corona接受的基因疗法,有可能从临床试验走向临床使用。近期一个独立的专家委员会以16:0投票一致通过,推荐FDA批准的Spark Therapeutics公司的luxturna基因疗法。FDA最晚将在2018年1月12日之前决定是否审批。
迄今为止,该疗法已取得显著效果。二十多个孩子和成年人因为这项疗法而改善了视力。但问题是它的效果是否持久,需要多少钱。FDA在本月早些时候发布的一份文件指出,目前还没有长期的数据可用。至于价格,一位分析师的预测把它的价格定在每只眼40万美元左右,而另一些分析师估计,这两只眼睛的价格可能高达100万美元。
几十年来,基因治疗被认为是治疗和潜在治愈严重遗传疾病的方法,被评为2017年10项突破性技术。传统的基因治疗方法是使用一种经过改造的病毒将一个健康的基因复制到一个有缺陷的病人身上。这种方法的目的是纠正疾病的遗传根源,而不是像大多数药物一样仅仅改善症状。
基因治疗2.0:2017年10大突破性技术之一
基因治疗2.0
-
突破性:美国首个正在审批流程中的基因疗法。
-
意义何在:成千上万的疾病源于单个基因的错误。新的基因治疗方法可以治愈他们。
几十年以来,研究人员一直追求着基因治疗的梦想。这个想法很优雅:使用设计的病毒将健康的基因拷贝到有缺陷的病人身上。但直到最近,基因治疗产生的失望远远多于成功。当1999年一名18岁的有肝脏疾病的患者在基因治疗试验中死亡时,整个研究领域都放慢了脚步。
基因治疗发展时间线:
但是现在,关键的难题已经解决了,基因疗法即将治愈毁灭性的遗传疾病。两个基因疗法治疗遗传性疾病的药物strimvelis和Glybera在欧洲已经获得监管部门的批准。在美国,Spark Therapeutics可能是第一个有基因治疗上市的公司;它有一种治疗渐进性失明的基因治疗方法。其他在研发中的基因治疗包括试图治愈血友病和缓解导致皮肤病大疱性表皮松解症的研究。
修复罕见的疾病,这本身就令人印象深刻,可能仅仅是个开始。研究人员正在研究的基因治疗临床试验中约包括40至50种不同的疾病。此外,除了治疗单基因功能紊乱引起的疾病外,研究人员还希望将这些疗法应用于更常见的疾病,如老年痴呆症、糖尿病、心力衰竭和癌症。甚至哈佛遗传学家说,总有一天,每个人都可以接受基因疗法来对抗衰老的影响。
早期基因治疗失败的部分原因是基因转运到细胞内机制出了问题。1990年,一位四岁的患有严重联合免疫缺陷(SCID)的女孩接受了美国国立卫生研究院的科学家们的治疗,他们从她身上提取了白细胞,将她错误基因的正常拷贝插入他们体内,然后给她注射了校正后的细胞。但后来不同类型的SCID病人接受基因治疗后患上了白血病。新的遗传物质和携带它进入细胞的病毒被送到了基因组的错误部分,在一些病人身上打开了致癌基因的开关。在死于基因疗法的18岁的肝脏患者的案例中,用于转运功能基因的病毒注入他的细胞后,使他的免疫系统进入过度运转,导致多器官功能衰竭和脑死亡。
基因疗法的研究人员已经通过使用更有效的方法,将新的遗传物质运送到细胞中的病毒克服了许多早期研究中出现的问题。
图:20世纪60年代,科学家发现了可以用来切割DNA序列并将它们固定在试管壁上的酶,这使得科学家产生了基因治疗的想法。
图:20世纪70年代科学家尝试利用病毒向动物中引入新基因。
图:1990年一个四岁的(图右下)患有遗传病严重联合免疫缺陷SCID的女孩接受了基因治疗,SCID使得她不能抵抗感染。但是其他患有这种疾病的孩子接受不同的基因治疗后患上了白血病。
图:1999 Jesse Gelsinger, 18岁,是第一个死于基因治疗临床试验的患者(用于转运功能基因的病毒注入他的细胞后,使他的免疫系统进入过度运转,导致多器官功能衰竭和脑死亡)
2007-2008年,患有遗传性视网膜疾病莱伯先天性黑朦的患者接受基因疗法治疗后视力视乎得到了提高。然而,几年后,研究人员在《新英格兰医学杂志》上报道,一些患者的视力已经开始衰退。
2012欧洲药品管理局批准了第一种基因治疗药物Glybera来治疗遗传性疾病脂蛋白脂酶缺乏,脂蛋白脂酶缺乏会造成脂肪在血液中堆积。
2016年5月,欧洲监管机构的批准了第二个基因治疗strimveli来治疗一种严重联合免疫缺陷。
2017或2018一种遗传性疾病的基因治疗可能首次在美国获得批准。
但基因治疗目前仍存在若干挑战。虽然已经为一些相对罕见的疾病研发了基因治疗,但是为更常见的、具有复杂的遗传原因的疾病提供疗法将要困难得多。在像SCID和血友病这样的疾病中,科学家们知道确切的导致疾病的基因变异。但是像阿尔茨海默氏症、糖尿病和心力衰竭、癌症之类的疾病涉及多种基因,且同样的基因并非参与到所有人的疾病中。尽管如此,对一些患者来讲,基因治疗的成功已经是真实的,而不是传说。
基因治疗将为癌症治疗带来新曙光
经过科学家数十年的不懈努力,几个单基因遗传性疾病的基因疗法的成功获批,提示在基因治疗领域已经取得了重大的突破。癌症也是一种基因疾病,虽然涉及的基因较多,基因的改变和基因之间的关系也非常复杂。但毕竟冰山被成功的揭开了一角,癌症治疗的曙光乍现。相信通过科学家的不断努力,癌症的基因治疗必将走向临床,造福广大的患者。