检测复发性GBM免疫疗法效果的报告基因成像
【Ref: Keu KV, et al. Sci Transl Med. 2017 Jan 18;9(373). pii: eaag2196. doi: 10.1126/scitranslmed.aag2196.】
免疫疗法治疗晚期肿瘤可能有巨大潜力,但部分肿瘤细胞能够逃过免疫监视并产生抵抗。因此需要有免疫治疗疗效评价标准(irRC)和非侵袭性的技术来早期判断免疫疗法的疗效。近期,美国斯坦福大学的Khun Visith Keu等对7例复发性脑胶质瘤患者进行免疫疗法的报告基因成像研究,结果发表在2017年1月《Science Translational Medicine》上。
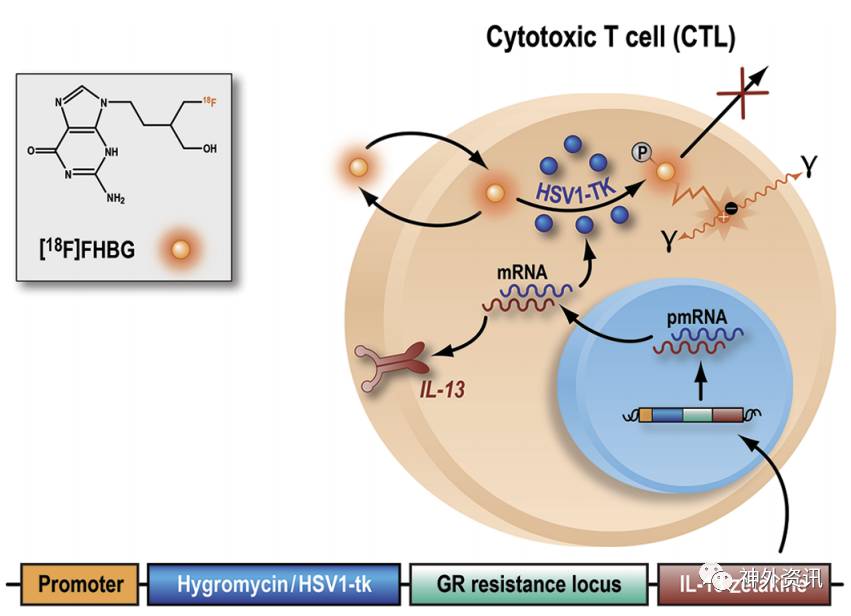
该研究通过基因改造的方法,将病毒导入自体或者异体的细胞毒性T细胞(cytotoxic T cell,CTL)中。IL-13嵌合抗原受体(chimeric antigen receptor,CAR)可使CTL特异性地靶向IL-13Rα2,表达于50%以上的胶质母细胞瘤(GBM)表面受体,而不表达于正常大脑组织。
[18F]FHBG是疱疹病毒药物喷昔洛韦(ganciclovir)的类似物。喷昔洛韦的作用靶点为Ⅰ型单纯疱疹病毒胸苷激酶(HSV1-tk),HSV1-tk同时起成像报告基因和自杀基因的作用。HSV1-tk将[18F]FHBG磷酸化为[18F]FHBG单磷酸盐。在哺乳动物细胞中,[18F]FHBG单磷酸盐又转化为[18F]FHBG三磷酸盐。[18F]FHBG三磷酸盐对细胞具有毒性,可以抑制DNA聚合酶等促使细胞死亡。CTL死亡后也会导致周围的肿瘤细胞死亡。未磷酸化的[18F]FHBG可以自由出入细胞,但被磷酸化的[18F]FHBG困在细胞之中。HSV1-tk将[18F]FHBG酶磷酸化的速率1000余倍于哺乳动物普通细胞中的激酶。因此,被改造过的CTL中含有大量的[18F]FHBG单磷酸盐,具有强烈的信号。而在其他细胞中,由于[18F]FHBG可以自由出入,其含量很少,所以背景信号较弱。
[18F]FHBG带有18F,能够通过正电子发射计算机断层扫描(PET)对有HSV1-tk表达的细胞进行成像。改造的CTL注入复发性高级别胶质瘤患者体内后,通过PET成像检测[18F]FHBG判断CTL迁徙、存活及增殖情况,从而反映免疫疗法的治疗效果(图1)。
图1. HSV1-tk病毒及[18F]FHBG监测原理图。
该研究招募的7例复发性高级别胶质瘤患者,平均年龄为57±8岁。在试验过程中,无1例因为 [18F]FHBG和CTL的注射而出现危及生命的症状。大部分患者在接受最后一次CTL注射的一年内死亡。
通过比较注射CTL前后标准化摄取值(standardized uptake value,SUV)的变化来定量地评估[18F]FHBG的放射性强度和分布情况。由于[18F]FHBG不能透过血脑屏障,正常大脑组织的SUV在注射CTL前后无明显差异,背景值很低。胶质瘤附近的血脑屏障结构受到破坏,[18F]FHBG则在胶质瘤内有明显的累积。分析注射位点处肿瘤的[18F]FHBG信号变化发现,6号患者的成像表现为感兴趣体积(volume of interest,VOI)的大小并无变化,但其中大部分像素点的值均有显著地增加,表现为SUV分布图右移。CTL注射后,VOI中各个像素点的SUV之和从4.1增至8.4。2号患者的结果类似,VOI中各个像素点的SUV之和从10.1增至20.3。在7号患者中,SUV分布的中位数并未发生明显的变化,而VOI的体积显著扩大促使总体的[18F]FHBG信号增加3.7倍,从注射前的1.8增至注射后的6.8(图2)。在多病灶患者中,远离注射位点未接受CTL注射病灶处的[18F]FHBG信号,总体上小幅度的增加,从1.6增至2.7;VOI的体积也小幅度的扩大;该结果暗示,CTL具有从注射位点向远距离的肿瘤病灶迁徙的能力。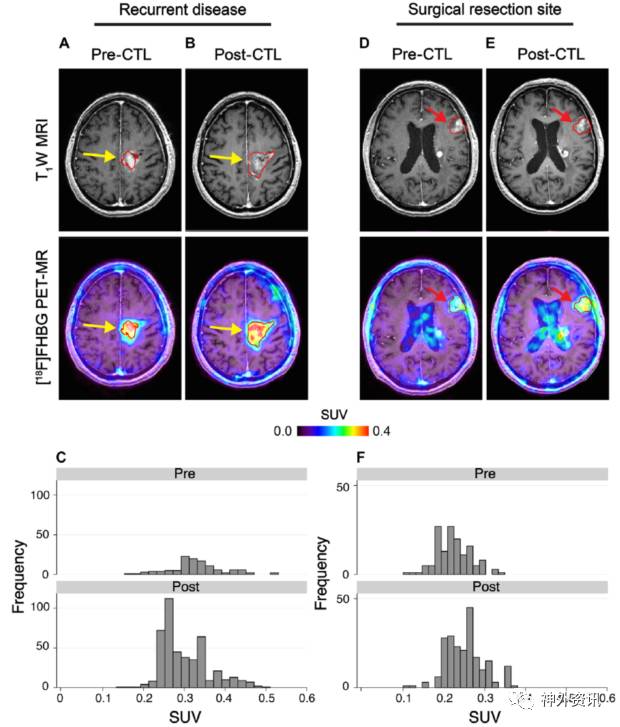
综上所述,该研究结果表明,利用特殊的PET示踪剂[18F]FHBG,对CTL表达的HSV1-tk报告基因进行成像,可以检测CAR治疗高级别脑胶质瘤的效果。
(上海交通大学医学院Rainy编译,复旦大学附属华山医院陈灵朝博士审校,《神外资讯》主编复旦大学附属华山医院陈衔城教授终审)