FDA批准SMA基因治疗药物SPINRAZA
在2016年即将画上句号之时,好消息再次传来。就在圣诞节来临之际,FDA批准了IONIS公司SMA反义核苷酸治疗药物SPINRAZA。FDA突破常规的快速批准,似乎是铁了心要扮演一回圣诞老人,为全世界的SMA患者和所有罕见病患者送来一份充满希望的大礼包。
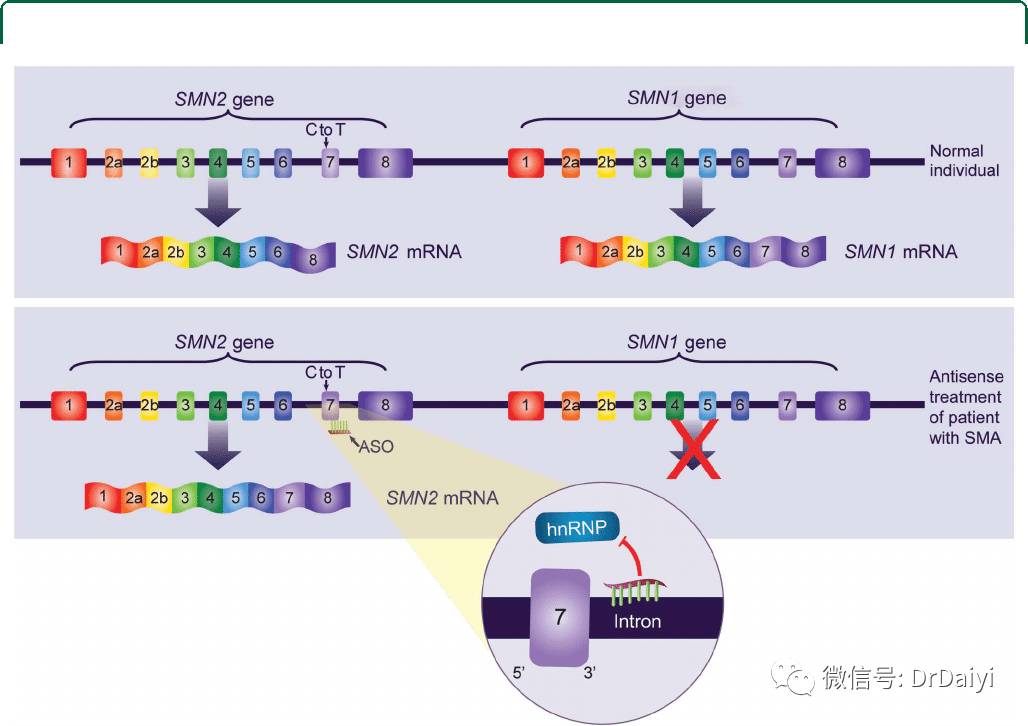
SPINRAZA是一种反义核苷酸,通过与SMN2外显子7的剪切位点结合,改变SMN2基因剪切,生成更能替代SMN1基因功能的蛋白产物,从而达到治疗疾病的作用。SPINRAZA在2011年才开始第一次在人体进行临床试验,短短5年时间,就获得FDA批准,不得不说是一个奇迹。
FDA本次批准SPINRAZA做的干净利落,完全没有DMD外显子跳跃治疗药物Eteplirsen批准时的纠结和犹豫,而且一次性批准SPINRAZA用于所有SMA患者,包括儿童和成人。究其原因,在于SPINRAZA的临床试验结果实在是太漂亮了,超出所有人预料,甚至IONIS公司自己都没有想到。在婴儿型SMA患者临床试验ENDEAR中,试验中期数据分析就见到明显治疗效果,临床试验提前终止。在晚发型SMA患者(SMA2)临床试验CHERISH中,再次在中期数据分析中发现明确疗效,再次提前终止临床试验。这一结果刚刚发表在国际著名学术期刊LANCET上。(http://www.thelancet.com/journals/lancet/article/PIIS0140-6736(16)31408-8/fulltext)
正是在这样强有力的结果面前,FDA也加快了自己的步伐,快速批准了SPINRAZA,我们已经能够FDA网站上看到SPINRAZA批准应用的药品信息。(http://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=209531)BIOGEN公司也信心满满的表示,准备在一周之内就将SPINRAZA运输至相关医院,让SMA患者有药可用。
基因治疗的大门已经打开。一年之中,遗传性神经肌肉病中的两大疾病,DMD和SMA都先后拥有了FDA批准的第一个基因治疗药物,我们为DMD患者和SMA患者高兴,更应该看到的是,对于所有罕见病患者,2016年都意义非凡。2016年作为“基因治疗正式临床应用元年”,必将永远被人们所铭记。